Este kit de ensayo ELISA cAMP colorimétrico Screen Quest™ proporciona un método sensible para detectar la actividad de la adenilato ciclasa en un sistema de ensayo bioquímico o basado en células.
Descripción
La adenosina 3′, 5′ monofosfato cíclico (cAMP) es un segundo mensajero importante en la transducción de señales intracelulares. El control de los niveles de AMPc es una de las formas más comunes de detectar agonistas y antagonistas de los GPCR.
El kit de ensayo de cAMP ELISA colorimétrico Screen Quest™ se basa en la competencia entre el cAMP marcado con HRP y el cAMP no marcado. HRP-cAMP es desplazado del complejo de anticuerpos HRP-cAMP/anti-cAMP por cAMP libre no marcado. En ausencia de cAMP, el conjugado HRP-cAMP se une exclusivamente al anticuerpo anti-cAMP. Sin embargo, el cAMP libre no marcado en la muestra de prueba compite por el anticuerpo anti-cAMP con el conjugado de anticuerpo HRP-cAMP, por lo tanto, inhibe la unión de HRP-cAMP al anticuerpo anti-cAMP.
Nuestro kit de ensayo ELISA cAMP colorimétrico Screen Quest™ proporciona un método sensible para detectar la actividad de la adenilato ciclasa en un sistema de ensayo bioquímico o basado en células. En comparación con otros kits de ensayo ELISA cAMP, nuestro kit elimina el tedioso paso de acetilación. El kit utiliza Amplite® Green como sustrato colorimétrico para cuantificar la actividad HRP.
El ensayo se puede realizar en un conveniente formato de placa de microtitulación de 96 pocillos o de 384 pocillos.
| Catalogo | Producto | Presentación |
|---|---|---|
| AAT-36370 | Screen Quest™ Colorimetric ELISA cAMP Assay Kit | 1 placa |
| AAT-36371 | Screen Quest™ Colorimetric ELISA cAMP Assay Kit | 10 placas |
Importante: Solo para uso en investigación (RUO).
Plataforma
Lector de Microplacas de Absorbancia
| Absorbancia | 405, 650 o 740 nm |
| Placa recomendada | Fondo claro (Componente F) |
Componentes
| Componente A: cAMP Standard | 1 vial (33 µg) |
| Componente B: Buffer de ensayo | 1 botella (20 mL) |
| Componente C: HRP-cAMP Conjugate | 1 vial |
| Componente D: 10X Wash Solution | 1 botella (10 mL) |
| Componente E: Cell Lysis Buffer | 1 botella (10 mL) |
| Componente F: Anti-cAMP Ab Coated 96-Well Plate | 1 placa |
| Componente G: Amplite™ Green | 1 botella (10 mL) |
PREPARACION DE SOLUCION DE STOCK
A menos que se indique lo contrario, todas las soluciones madre no utilizadas deben dividirse en alícuotas de un solo uso y almacenarse a -20 °C después de la preparación. Evite los ciclos repetidos de congelación y descongelación.
1. Solución madre de AMPc (100 µM): Agregue 1 ml de buffer de ensayo (componente B) al vial de estándar cAMP (componente A).
2. Solución madre de conjugado HRP-AMPc (50X): Agregue 55 µL (catálogo 36370) o 550 µl (catálogo 36371) de buffer de ensayo (componente B) en el vial de conjugado HRP-AMPc (componente C). Nota: La solución madre del conjugado 50X HRP-cAMP sin usar debe dividirse en alícuotas de un solo uso y almacenarse a -20 oC.
3. Solución de lavado (1X): Agregue 1 ml de solución de lavado 10X (componente D) a 9 ml de agua destilada.
PREPARACION DE SOLUCION ESTANDAR
cAMP standard
Para su conveniencia use el Planeador Serial de Dilucion: https://www.aatbio.com/tools/serial-dilution/36370
Realice diluciones en serie 1:10, 1:100 y 1:3 de estándares de AMPc en buffer de ensayo (componente B) para obtener AMPc de 10,000, 100, 30, 10, 3, 1, 0.3, 0.1, 0.03, 0.01 y 0.003 nM soluciones diluidas. Conservar en hielo o 4°C.
PREPARACION DE SOLUCION DE TRABAJO
Solución de trabajo del conjugado HRP-cAMP:
Realice una dilución 1:50 con buffer de ensayo (componente B) para obtener una solución de trabajo de conjugado HRP-cAMP 1X antes de su uso. Guárdelo en hielo o a 4°C. Nota: 25 µL de solución de trabajo de conjugado 1X HRP-cAMP es suficiente para un punto de ensayo; prepare adecuadamente el volumen para un solo uso.
Para obtener guias sobre la preparación de muestras de células, visite: https://www.aatbio.com/resources/guides/cell-sample-preparation.html
Imagenes

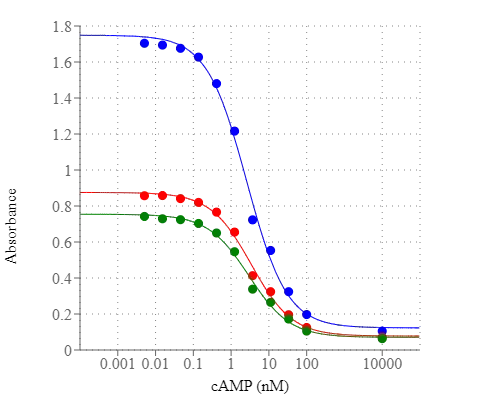
Figura 1. La respuesta a la dosis de AMPc se midió con el kit de ensayo de AMPc ELISA colorimétrico Screen Quest™ en una placa transparente de 96 pocillos con un lector de microplacas SpectraMax. La Absorbancia se puede leer a 405 nm (línea azul), 650 nm (línea roja) o 740 nm (línea verde), los datos de la figura B son de la incubación con Amplite® Green durante 3 horas.

Figura 2. La respuesta a la dosis de AMPc se midió con el kit de ensayo de AMPc ELISA colorimétrico Screen Quest™ en una placa transparente de 96 pocillos con un lector de microplacas SpectraMax. R: El kit puede detectar cAMP tan bajo como 0.1 nM en un volumen de reacción de 100 µL a 405 nm después de la incubación con Amplite® Green durante 1 hora (línea azul) y 3 horas (línea roja).

Figura 3. La reducción de la migración de BTEC depende del aumento de [cAMP]i. (A) producción de AMPc tras la estimulación con diferentes agonistas purinérgicos o CPA. ATP 100 μM y otros agonistas purinérgicos antimigratorios inducen un fuerte aumento en el nivel de AMPc intracelular después de 15′ de tratamiento, como se muestra en la tabla A (los datos de al menos tres experimentos independientes se normalizan al control). (B) Los niveles altos de AMPc pueden reducir la migración de BTEC en el ensayo de cicatrización de heridas. Se utilizaron diferentes inductores del aumento de cAMP intracelular: Forskolin 10 μM (FK), 8-Br-cAMP 500 μM e IBMX 100 μM. Los datos se normalizan en CNTRL positivo a las 8 horas y se expresan como media ± S.E.M. Prueba de Wilcoxon: *p < 0.001 vs CNTRL; §p < 0,001 frente a ATP 100 μM; #p < 0.001. (C,i) Tinción de actina y paxilina en células tratadas con FK 10 μM o no (CNTRL) durante 5′. Las flechas en (C,i) indican la distribución de los filamentos de actina y se evaluó la intensidad de la fluorescencia de la faloidina a lo largo del eje de la célula principal (líneas blancas en las figuras). Barra de escala = 10 μm (C,ii) Cuantificación de la localización de actina cortical. (C, iii) Cuantificación de la densidad de paxilina tras el tratamiento con FK. (C,iv) Área total medida para cada condición. Los datos obtenidos de tres experimentos independientes se expresan como media ± S.E.M. Prueba de Wilcoxon: *p < 0.001 vs CNTRL. (D) Efecto sobre la migración de BTEC (cicatrización de heridas) de diferentes moduladores de adenilil ciclasa (ddAdo, NaHCO3), activador de EPAC-1 (8-CPT) e inhibidor de PKA (H89). La línea punteada representa la inhibición inducida por ATP. Los datos se normalizan en CNTRL positivo a las 8 horas y se expresan como media ± S.E.M. Prueba de Wilcoxon: *p < 0.001 vs CNTRL; §p < 0,001 frente a ATP 100 μM; #p < 0.001. Fuente: La activación de los receptores purinérgicos P2X7 y P2Y11 inhibe la migración y normaliza las células endoteliales derivadas de tumores a través de la señalización de AMPc por Avanzato et al., Scientific Reports, septiembre de 2016.
Productos Relacionados
Bibliografía
Activation of P2X7 and P2Y11 purinergic receptors inhibits migration and normalizes tumor-derived endothelial cells via cAMP signaling
Authors: Avanzato, D and Genova, T and Pla, A Fiorio and Bernardini, M and Bianco, S and Bussolati, B and Mancardi, D and Giraudo, E and Maione, F and Cassoni, P and others, undefined
Journal: Scientific Reports (2016)
The M2 muscarinic receptors are essential for signaling in the heart left ventricle during restraint stress in mice
Authors: Tomankova, Hana and Valuskova, Paulina and Varejkova, Eva and Rotkova, Jana and Benes, Jan and Myslivecek, Jaromir
Journal: Stress (2015)
THE EFFECTS OF RESTRAINT STRESS ON HEART M
Authors: Valu{\v{s}}kov{\’a}, Paulina and Tomankov{\’a}, Hana and Rotkov{\’a}, Jana and Va{\v{r}}ejkov{\’a}, Eva and Bene{\v{s}}, Jan
Referencias
Ver todas las 132 referencias: Citation Explorer
cAMP-Induced Histones H3 Dephosphorylation Is Independent of PKA and MAP Kinase Activations and Correlates With mTOR Inactivation
Authors: Rodriguez P, Rojas J.
Journal: J Cell Biochem (2016): 741
Changes in the Arabidopsis thaliana Proteome Implicate cAMP in Biotic and Abiotic Stress Responses and Changes in Energy Metabolism
Authors: Alqurashi M, Gehring C, Marondedze C.
Journal: Int J Mol Sci (2016): 852
Role of the cAMP Pathway in Glucose and Lipid Metabolism
Authors: Ravnskjaer K, Madiraju A, Montminy M.
Journal: Handb Exp Pharmacol (2016): 29
Odor-induced cAMP production in Drosophila melanogaster olfactory sensory neurons
Authors: Miazzi F, Hansson BS, Wicher D.
Journal: J Exp Biol (2016): 1798
A cardiac mitochondrial cAMP signaling pathway regulates calcium accumulation, permeability transition and cell death
Authors: Wang Z, Liu D, Varin A, Nicolas V, Courilleau D, Mateo P, Caubere C, Rouet P, Gomez AM, V and ecasteele G, Fischmeister R, Brenner C.
Journal: Cell Death Dis (2016): e2198
The pleiotropic role of exchange protein directly activated by cAMP 1 (EPAC1) in cancer: implications for therapeutic intervention
Authors: Almahariq M, Mei FC, Cheng X.
Journal: Acta Biochim Biophys Sin (Shanghai) (2016): 75
A cAMP Biosensor-Based High-Throughput Screening Assay for Identification of Gs-Coupled GPCR Ligands and Phosphodiesterase Inhibitors
Authors: Vedel L, Brauner-Osborne H, Mathiesen JM.
Journal: J Biomol Screen (2015): 849
Imaging alterations of cardiomyocyte cAMP microdomains in disease
Authors: Froese A, Nikolaev VO.
Journal: Front Pharmacol (2015): 172
Cardiac Hypertrophy Is Inhibited by a Local Pool of cAMP Regulated by Phosphodiesterase 2
Authors: Zoccarato A, Surdo NC, Aronsen JM, Fields LA, Mancuso L, Dodoni G, Stangherlin A, Livie C, Jiang H, Sin YY, Gesellchen F, Terrin A, Baillie GS, Nicklin SA, Graham D, Szabo-Fresnais N, Krall J, V and eput F, Movsesian M, Furlan L, Corsetti V, Hamilton G, Lefkimmiatis K, Sjaastad I, Zaccolo M.
Journal: Circ Res (2015): 707
cAMP controls the balance of the propulsive forces generated by the two flagella of Chlamydomonas
Authors: Saegusa Y, Yoshimura K.
Journal: Cytoskeleton (Hoboken) (2015): 412
Application Notes (en Ingles)
A Meta-Analysis of Common Calcium Indicators
A New Protein Crosslinking Method for Labeling and Modifying Antibodies
A Novel Fluorescent Probe for Imaging and Detecting Hydroxyl Radical in Living Cells
Abbreviation of Common Chemical Compounds Related to Peptides
Annexin V
AssayWise (en Ingles)
HRP Antibody Labeling Using Buccutite™ Crosslinking Technology
iFluor® 700 Dyes
Hydroxyl Radical Detection
Peroxidase Detection
Buccutite™ Conjugation Kits: Quick and Easy Antibody Labeling